V sodobni medicini so se antibiotiki izkazali za enega najpomembnejših dosežkov, saj so dramatično znižali pojavnost in umrljivost, povezano z mikrobnimi okužbami. Njihova sposobnost spreminjanja kliničnih izidov bakterijskih okužb je podaljšala pričakovano življenjsko dobo neštetih bolnikov. Antibiotiki so ključnega pomena pri kompleksnih medicinskih posegih, vključno z operacijami, vstavitvijo vsadkov, presaditvami in kemoterapijo. Vendar pa je pojav patogenov, odpornih na antibiotike, vse večja zaskrbljenost, ki sčasoma zmanjšuje učinkovitost teh zdravil. Primeri odpornosti na antibiotike so bili dokumentirani v vseh kategorijah antibiotikov, saj se pojavljajo mikrobne mutacije. Selekcijski pritisk, ki ga izvajajo protimikrobna zdravila, je prispeval k porastu odpornih sevov, kar predstavlja velik izziv za globalno zdravje.
Za boj proti perečemu vprašanju odpornosti na protimikrobna zdravila je bistveno izvajanje učinkovitih politik za nadzor okužb, ki omejujejo širjenje odpornih patogenov in hkrati zmanjšujejo uporabo antibiotikov. Poleg tega obstaja nujna potreba po alternativnih metodah zdravljenja. Hiperbarična kisikova terapija (HBOT) se je v tem kontekstu izkazala kot obetavna metoda, ki vključuje vdihavanje 100-odstotnega kisika pri določenih ravneh tlaka za določeno časovno obdobje. HBOT, ki se uporablja kot primarno ali dopolnilno zdravljenje okužb, lahko ponudi novo upanje pri zdravljenju akutnih okužb, ki jih povzročajo patogeni, odporni na antibiotike.
Ta terapija se vse pogosteje uporablja kot primarno ali alternativno zdravljenje različnih stanj, vključno z vnetjem, zastrupitvijo z ogljikovim monoksidom, kroničnimi ranami, ishemičnimi boleznimi in okužbami. Klinična uporaba HBOT pri zdravljenju okužb je obsežna in bolnikom zagotavlja neprecenljive prednosti.

Klinična uporaba hiperbarične kisikove terapije pri okužbah
Trenutni dokazi močno podpirajo uporabo HBOT, tako kot samostojnega kot dodatnega zdravljenja, kar prinaša znatne koristi za okužene bolnike. Med HBOT se lahko tlak kisika v arterijski krvi dvigne na 2000 mmHg, posledično visok gradient tlaka med kisikom in tkivom pa lahko zviša raven kisika v tkivu na 500 mmHg. Takšni učinki so še posebej dragoceni pri spodbujanju celjenja vnetnih odzivov in motenj mikrocirkulacije, opaženih v ishemičnih okoljih, ter pri obvladovanju kompartmentnega sindroma.
HBOT lahko vpliva tudi na stanja, ki so odvisna od imunskega sistema. Raziskave kažejo, da lahko HBOT zavira avtoimunske sindrome in antigensko povzročene imunske odzive, s čimer pomaga ohranjati toleranco presadka z zmanjšanjem krvnega obtoka limfocitov in levkocitov, hkrati pa modulira imunske odzive. Poleg tega HBOTpodpira celjenjepri kroničnih kožnih lezijah s spodbujanjem angiogeneze, ključnega procesa za boljše okrevanje. Ta terapija spodbuja tudi tvorbo kolagena, ki je bistvena faza pri celjenju ran.
Posebno pozornost je treba nameniti nekaterim okužbam, zlasti globokim in težko ozdravljivim okužbam, kot so nekrotizirajoči fasciitis, osteomielitis, kronične okužbe mehkih tkiv in infekcijski endokarditis. Ena najpogostejših kliničnih uporab HBOT je pri okužbah kože in mehkih tkiv ter osteomielitisu, povezanih z nizko ravnjo kisika, ki jih pogosto povzročajo anaerobne ali odporne bakterije.
1. Okužbe diabetičnega stopala
Diabetično stopaloRazjede so pogost zaplet pri sladkornih bolnikih, ki prizadenejo do 25 % te populacije. V teh razjedah se pogosto pojavijo okužbe (predstavljajo 40 %–80 % primerov) in vodijo do povečane obolevnosti in umrljivosti. Okužbe diabetičnega stopala (ODS) običajno sestavljajo polimikrobne okužbe z različnimi anaerobnimi bakterijskimi patogeni. Različni dejavniki, vključno z okvarami delovanja fibroblastov, težavami s tvorbo kolagena, celičnimi imunskimi mehanizmi in delovanjem fagocitov, lahko ovirajo celjenje ran pri sladkornih bolnikih. Več študij je ugotovilo, da je oslabljena oksigenacija kože močan dejavnik tveganja za amputacije, povezane z ODS.
Kot ena od trenutnih možnosti za zdravljenje DFIPoročali so, da HBOT znatno pospeši celjenje razjed na diabetičnem stopalu, kar posledično zmanjša potrebo po amputacijah in zapletenih kirurških posegih. Ne le da zmanjšuje potrebo po posegih, ki zahtevajo veliko virov, kot so operacije režnjev in presaditev kože, temveč predstavlja tudi nižje stroške in minimalne stranske učinke v primerjavi s kirurškimi možnostmi. Študija Chena in sodelavcev je pokazala, da je več kot 10 sej HBOT pri sladkornih bolnikih privedlo do 78,3-odstotnega izboljšanja stopnje celjenja ran.
2. Nekrotizirajoče okužbe mehkih tkiv
Nekrotizirajoče okužbe mehkih tkiv (NSTI) so pogosto polimikrobne, običajno nastanejo zaradi kombinacije aerobnih in anaerobnih bakterijskih patogenov in so pogosto povezane s tvorbo plinov. Čeprav so NSTI relativno redke, imajo zaradi hitrega napredovanja visoko stopnjo umrljivosti. Pravočasna in ustrezna diagnoza ter zdravljenje sta ključnega pomena za doseganje ugodnih izidov, zato je bila HBOT priporočena kot dodatna metoda za obvladovanje NSTI. Čeprav o uporabi HBOT pri NSTI še vedno obstajajo spori zaradi pomanjkanja prospektivnih kontroliranih študij,dokazi kažejo, da je to lahko povezano z izboljšano stopnjo preživetja in ohranitvijo organov pri bolnikih z NSTIRetrospektivna študija je pokazala znatno zmanjšanje stopnje umrljivosti med bolniki z NSTI, ki prejemajo HBOT.
1.3 Okužbe kirurškega mesta
Infekcije kirurškega posega (SSI) lahko razvrstimo glede na anatomsko mesto okužbe in jih lahko povzročijo različni patogeni, vključno z aerobnimi in anaerobnimi bakterijami. Kljub napredku pri ukrepih za nadzor okužb, kot so tehnike sterilizacije, uporaba profilaktičnih antibiotikov in izboljšave kirurških praks, SSI ostajajo vztrajen zaplet.
V enem pomembnem pregledu so raziskovali učinkovitost HBOT pri preprečevanju globokih poškodb kirurškega posega v rano (SSI) pri operacijah živčno-mišične skolioze. Predoperativna HBOT lahko znatno zmanjša pojavnost SSI in olajša celjenje ran. Ta neinvazivna terapija ustvarja okolje, kjer so ravni kisika v tkivih rane povišane, kar je povezano z oksidativnim uničevanjem patogenov. Poleg tega obravnava znižane ravni kisika v krvi, ki prispevajo k razvoju SSI. Poleg drugih strategij za nadzor okužb je HBOT priporočljiva zlasti za operacije s čisto kontaminacijo, kot so kolorektalni posegi.
1.4 Opekline
Opekline so poškodbe, ki jih povzročijo ekstremna vročina, električni tok, kemikalije ali sevanje, in lahko povzročijo visoko stopnjo obolevnosti in umrljivosti. HBOT je koristen pri zdravljenju opeklin, saj povečuje raven kisika v poškodovanih tkivih. Čeprav študije na živalih in klinične študije kažejo mešane rezultate gledeučinkovitost HBOT pri zdravljenju opeklinŠtudija, v kateri je sodelovalo 125 bolnikov z opeklinami, je pokazala, da HBOT ni pokazala pomembnega vpliva na stopnjo umrljivosti ali število opravljenih operacij, je pa skrajšala povprečni čas celjenja (19,7 dni v primerjavi s 43,8 dneva). Integracija HBOT s celovitim zdravljenjem opeklin bi lahko učinkovito nadzorovala sepso pri bolnikih z opeklinami, kar bi vodilo do krajšega časa celjenja in zmanjšane potrebe po tekočini. Vendar pa so za potrditev vloge HBOT pri zdravljenju obsežnih opeklin potrebne nadaljnje obsežne prospektivne raziskave.
1.5 Osteomielitis
Osteomielitis je okužba kosti ali kostnega mozga, ki jo pogosto povzročajo bakterijski patogeni. Zdravljenje osteomielitisa je lahko zahtevno zaradi relativno slabe prekrvavitve kosti in omejenega prodiranja antibiotikov v kostni mozeg. Za kronični osteomielitis so značilni vztrajni patogeni, blago vnetje in nekrotično tvorbo kostnega tkiva. Refraktorni osteomielitis se nanaša na kronične okužbe kosti, ki se nadaljujejo ali ponavljajo kljub ustreznemu zdravljenju.
Dokazano je, da HBOT znatno izboljša raven kisika v okuženih kostnih tkivih. Številne serije primerov in kohortne študije kažejo, da HBOT izboljša klinične izide pri bolnikih z osteomielitisom. Zdi se, da deluje prek različnih mehanizmov, vključno s povečanjem presnovne aktivnosti, zaviranjem bakterijskih patogenov, izboljšanjem učinkov antibiotikov, zmanjšanjem vnetja in spodbujanjem celjenja.procesov. Po HBOT kaže 60 % do 85 % bolnikov s kroničnim, neodzivnim osteomielitisom znake supresije okužbe.
1.6 Glivične okužbe
Po vsem svetu več kot tri milijone posameznikov trpi zaradi kroničnih ali invazivnih glivnih okužb, kar letno povzroči več kot 600.000 smrti. Izidi zdravljenja glivičnih okužb so pogosto ogroženi zaradi dejavnikov, kot so spremenjen imunski status, osnovne bolezni in značilnosti virulence patogenov. HBOT postaja privlačna terapevtska možnost pri hudih glivičnih okužbah zaradi svoje varnosti in neinvazivne narave. Študije kažejo, da bi lahko bil HBOT učinkovit proti glivičnim patogenom, kot sta Aspergillus in Mycobacterium tuberculosis.
HBOT spodbuja protiglivične učinke z zaviranjem nastajanja biofilma pri Aspergillusu, pri čemer je bila opažena povečana učinkovitost pri sevih, ki nimajo genov za superoksid dismutazo (SOD). Hipoksični pogoji med glivičnimi okužbami predstavljajo izziv za dostavo protiglivičnih zdravil, zato so povečane ravni kisika iz HBOT potencialno koristne, čeprav so potrebne nadaljnje raziskave.
Protimikrobne lastnosti HBOT
Hiperoksično okolje, ki ga ustvari HBOT, sproži fiziološke in biokemične spremembe, ki spodbujajo antibakterijske lastnosti, zaradi česar je učinkovito dodatno zdravljenje okužb. HBOT kaže izjemne učinke proti aerobnim bakterijam in pretežno anaerobnim bakterijam prek mehanizmov, kot so neposredno baktericidno delovanje, okrepitev imunskega odziva in sinergistični učinki s specifičnimi protimikrobnimi sredstvi.
2.1 Neposredni antibakterijski učinki HBOT
Neposredni antibakterijski učinek HBOT se v veliki meri pripisuje nastajanju reaktivnih kisikovih spojin (ROS), ki vključujejo superoksidne anione, vodikov peroksid, hidroksilne radikale in hidroksilne ione – vsi ti nastanejo med celičnim metabolizmom.
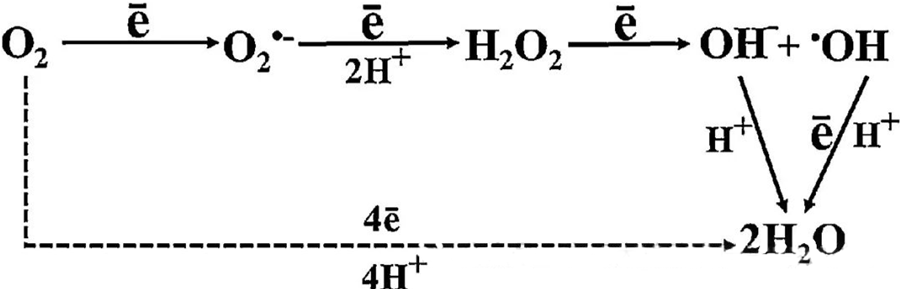
Interakcija med O₂ in celičnimi komponentami je bistvena za razumevanje, kako nastajajo ROS v celicah. V določenih pogojih, imenovanih oksidativni stres, se poruši ravnovesje med nastajanjem ROS in njihovo razgradnjo, kar vodi do povišanih ravni ROS v celicah. Nastajanje superoksida (O₂⁻) katalizira superoksid dismutaza, ki nato pretvori O₂⁻ v vodikov peroksid (H₂O₂). To pretvorbo dodatno okrepi Fentonova reakcija, ki oksidira Fe²⁺ in ustvari hidroksilne radikale (·OH) in Fe³⁺, s čimer se sproži škodljivo redoks zaporedje nastajanja ROS in poškodb celic.
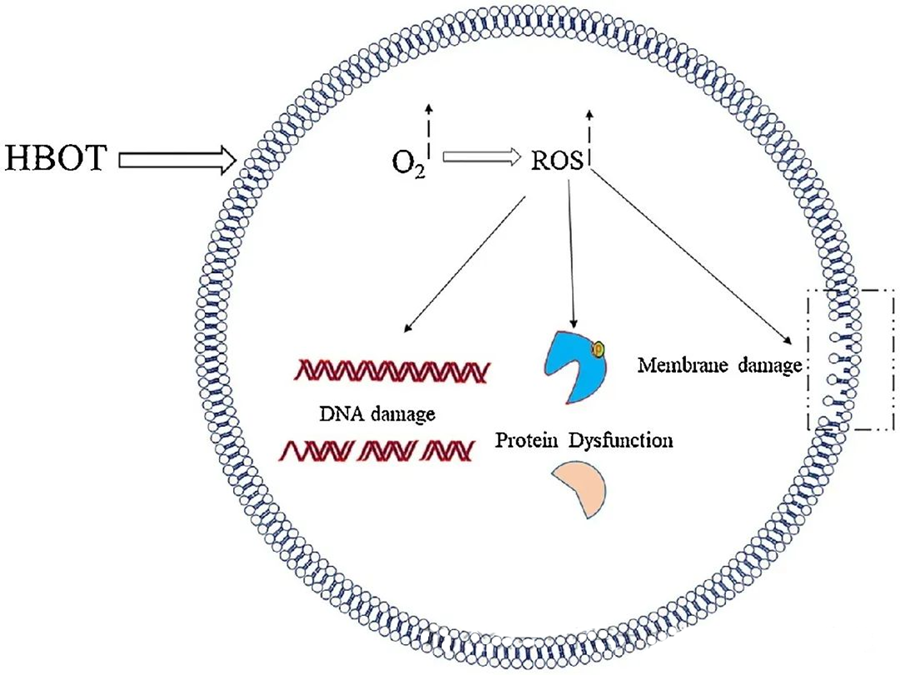
Toksični učinki ROS ciljajo na kritične celične komponente, kot so DNK, RNK, beljakovine in lipidi. Predvsem je DNK primarna tarča citotoksičnosti, ki jo posreduje H₂O₂, saj moti deoksiribozne strukture in poškoduje bazne sestave. Fizična škoda, ki jo povzročajo ROS, sega do vijačne strukture DNK, kar je lahko posledica lipidne peroksidacije, ki jo sprožijo ROS. To poudarja negativne posledice povišanih ravni ROS v bioloških sistemih.
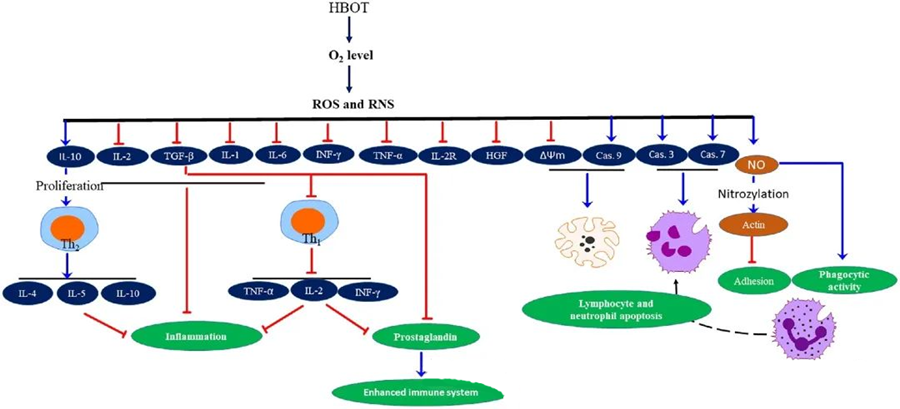
Protimikrobno delovanje ROS
ROS igrajo ključno vlogo pri zaviranju rasti mikrobov, kar dokazuje nastajanje ROS, ki ga povzroča HBOT. Toksični učinki ROS neposredno ciljajo na celične sestavine, kot so DNK, beljakovine in lipidi. Visoke koncentracije aktivnih kisikovih spojin lahko neposredno poškodujejo lipide, kar vodi do lipidne peroksidacije. Ta proces ogroža celovitost celičnih membran in posledično funkcionalnost membransko povezanih receptorjev in beljakovin.
Poleg tega beljakovine, ki so prav tako pomembne molekularne tarče ROS, doživijo specifične oksidativne modifikacije na različnih aminokislinskih ostankih, kot so cistein, metionin, tirozin, fenilalanin in triptofan. Na primer, dokazano je, da HBOT povzroča oksidativne spremembe v več beljakovinah v E. coli, vključno z elongacijskim faktorjem G in DnaK, in s tem vpliva na njihove celične funkcije.
Krepitev imunosti s pomočjo HBOT
Protivnetne lastnosti HBOTdokumentirane so bile, kar se je izkazalo za ključnega pomena za lajšanje poškodb tkiva in zaviranje napredovanja okužbe. HBOT pomembno vpliva na izražanje citokinov in drugih vnetnih regulatorjev, kar vpliva na imunski odziv. Različni eksperimentalni sistemi so opazili različne spremembe v izražanju genov in nastajanju beljakovin po HBOT, ki bodisi povečajo bodisi zmanjšajo rastne faktorje in citokine.
Med procesom HBOT povečane ravni O₂ sprožijo vrsto celičnih odzivov, kot sta zaviranje sproščanja provnetnih mediatorjev in spodbujanje apoptoze limfocitov in nevtrofilcev. Ta dejanja skupaj krepijo protimikrobne mehanizme imunskega sistema in s tem olajšajo celjenje okužb.
Poleg tega študije kažejo, da lahko povečane ravni O₂ med HBOT zmanjšajo izražanje provnetnih citokinov, vključno z interferonom-gama (IFN-γ), interlevkinom-1 (IL-1) in interlevkinom-6 (IL-6). Te spremembe vključujejo tudi znižanje razmerja med celicami CD4:CD8 T in modulacijo drugih topnih receptorjev, kar na koncu zviša ravni interlevkina-10 (IL-10), ki je ključnega pomena za preprečevanje vnetja in spodbujanje celjenja.
Protimikrobno delovanje HBOT je prepleteno s kompleksnimi biološkimi mehanizmi. Poročali so, da tako superoksid kot povišan krvni tlak nedosledno spodbujata antibakterijsko delovanje, ki ga povzroča HBOT, in apoptozo nevtrofilcev. Po HBOT izrazito povišanje ravni kisika poveča baktericidne sposobnosti nevtrofilcev, ki so bistveni sestavni del imunskega odziva. Poleg tega HBOT zavira adhezijo nevtrofilcev, ki jo posreduje interakcija β-integrinov na nevtrofilcih z medceličnimi adhezijskimi molekulami (ICAM) na endotelijskih celicah. HBOT zavira aktivnost nevtrofilnega β-2 integrina (Mac-1, CD11b/CD18) preko procesa, ki ga posreduje dušikov oksid (NO), kar prispeva k migraciji nevtrofilcev na mesto okužbe.
Natančna preureditev citoskeleta je potrebna, da nevtrofilci učinkovito fagocitirajo patogene. Dokazano je, da S-nitrozilacija aktina spodbuja polimerizacijo aktina, kar lahko po predhodnem zdravljenju s HBOT olajša fagocitno aktivnost nevtrofilcev. Poleg tega HBOT spodbuja apoptozo v človeških celičnih linijah T preko mitohondrijskih poti, pri čemer je bila opisana pospešena smrt limfocitov po HBOT. Blokiranje kaspaze-9 – brez vpliva na kaspazo-8 – je pokazalo imunomodulatorne učinke HBOT.
Sinergijski učinki HBOT z antimikrobnimi sredstvi
V klinični praksi se HBOT pogosto uporablja skupaj z antibiotiki za učinkovit boj proti okužbam. Hiperoksično stanje, doseženo med HBOT, lahko vpliva na učinkovitost nekaterih antibiotikov. Raziskave kažejo, da specifična baktericidna zdravila, kot so β-laktami, fluorokinoloni in aminoglikozidi, ne delujejo le prek inherentnih mehanizmov, temveč se delno zanašajo tudi na aerobni metabolizem bakterij. Zato sta prisotnost kisika in presnovne značilnosti patogenov ključnega pomena pri ocenjevanju terapevtskih učinkov antibiotikov.
Pomembni dokazi kažejo, da lahko nizke ravni kisika povečajo odpornost Pseudomonas aeruginosa na piperacilin/tazobaktam in da okolje z nizko vsebnostjo kisika prispeva tudi k povečani odpornosti Enterobacter cloacae na azitromicin. Nasprotno pa lahko nekatere hipoksične razmere povečajo občutljivost bakterij na tetraciklinske antibiotike. HBOT služi kot ustrezna dodatna terapevtska metoda, saj spodbuja aerobni metabolizem in reoksigenira hipoksično okužena tkiva, kar posledično poveča občutljivost patogenov na antibiotike.
V predkliničnih študijah je kombinacija HBOT – ki se je dajala dvakrat na dan 8 ur pri 280 kPa – skupaj s tobramicinom (20 mg/kg/dan) znatno zmanjšala bakterijsko obremenitev pri infekcijskem endokarditisu, ki ga povzroča Staphylococcus aureus. To dokazuje potencial HBOT kot pomožnega zdravljenja. Nadaljnje raziskave so pokazale, da je HBOT pri 37 °C in tlaku 3 ATA 5 ur znatno okrepil učinke imipenema proti Pseudomonas aeruginosa, okuženi z makrofagi. Poleg tega se je izkazalo, da je kombinirana metoda HBOT s cefazolinom učinkovitejša pri zdravljenju osteomielitisa, ki ga povzroča Staphylococcus aureus, v živalskih modelih v primerjavi s cefazolinom samim.
HBOT prav tako znatno poveča baktericidno delovanje ciprofloksacina proti biofilmom Pseudomonas aeruginosa, zlasti po 90 minutah izpostavljenosti. To povečanje je posledica nastajanja endogenih reaktivnih kisikovih spojin (ROS) in kaže povečano občutljivost pri mutantih z okvaro peroksidaze.
V modelih plevritisa, ki ga povzroča meticilin-rezistentni Staphylococcus aureus (MRSA), je skupni učinek vankomicina, teikoplanina in linezolida s HBOT pokazal znatno povečano učinkovitost proti MRSA. Metronidazol, antibiotik, ki se pogosto uporablja za zdravljenje hudih anaerobnih in polimikrobnih okužb, kot so okužbe diabetičnega stopala (DFI) in okužbe mesta kirurškega posega (SSI), je pokazal večjo protimikrobno učinkovitost v anaerobnih pogojih. Za raziskavo sinergijskih antibakterijskih učinkov HBOT v kombinaciji z metronidazolom so potrebne nadaljnje študije tako in vivo kot in vitro.
Protimikrobna učinkovitost HBOT na odporne bakterije
Z razvojem in širjenjem odpornih sevov tradicionalni antibiotiki sčasoma pogosto izgubijo svojo učinkovitost. Poleg tega se lahko HBOT izkaže za bistveno pri zdravljenju in preprečevanju okužb, ki jih povzročajo patogeni, odporni na več zdravil, in služi kot ključna strategija, kadar zdravljenje z antibiotiki ne uspe. Številne študije so poročale o pomembnih baktericidnih učinkih HBOT na klinično pomembne odporne bakterije. Na primer, 90-minutna seja HBOT pri 2 ATM je znatno zmanjšala rast MRSA. Poleg tega je HBOT v modelih razmerij okrepil antibakterijske učinke različnih antibiotikov proti okužbam z MRSA. Poročila so potrdila, da je HBOT učinkovit pri zdravljenju osteomielitisa, ki ga povzroča Klebsiella pneumoniae, ki proizvaja OXA-48, ne da bi bili potrebni dodatni antibiotiki.
Skratka, hiperbarična kisikova terapija predstavlja večplasten pristop k nadzoru okužb, saj krepi imunski odziv in hkrati povečuje učinkovitost obstoječih protimikrobnih sredstev. Z obsežnimi raziskavami in razvojem ima potencial za ublažitev učinkov odpornosti na antibiotike in ponuja upanje v nenehnem boju proti bakterijskim okužbam.
Čas objave: 28. februar 2025

